Hope?!
 Maladies auto-immunes : des nanoparticules stoppent leur évolution
Maladies auto-immunes : des nanoparticules stoppent leur évolution
Des nanoparticules couplées à un antigène spécifique ont réussi à arrêter une maladie équivalente à la sclérose en plaques chez des souris. Le procédé, qui consiste à reconfigurer le système immunitaire, pourrait également être appliqué à d’autres maladies auto-immunes, comme le diabète de type 1 ou certaines allergies.
C’est une histoire de finesse du réglage. Même si les maladies auto-immunes n’ont pas livré tous leurs secrets, on sait qu’elles se manifestent à cause de cellules de l’immunité appelées lymphocytes T (LT) qui font de l’excès de zèle en s’attaquant à des tissus sains de l’organisme, qu’elles considèrent comme étrangers.
En temps normal, les cellules naissent, vivent et meurent. Arrivées à cette dernière étape, elles intègrent la circulation avant d’être repérées et digérées par les macrophages, qui jouent le rôle d’éboueurs. Au niveau de la rate, ces macrophages rencontrent les LT et leur enseignent à distinguer les éléments du corps des éléments étrangers. Comment ? En présentant à leur surface les antigènes propres à l’individu qu’ils ont récupérés dans les cellules mortes.
Mais les LT connaissent parfois des difficultés d’apprentissage et attaquent des cellules de l’organisme, entraînant des maladies auto-immunes comme le diabète de type 1, les allergies ou la sclérose en plaques.
Remplacer des globules blancs par des nanoparticules
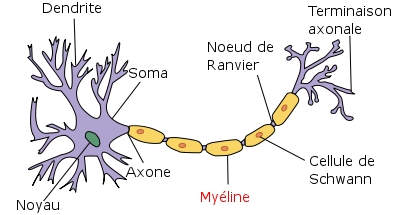
Dans cette maladie, c’est la gaine de myéline qui est victime des LT. Cette couche qui entoure les neurones et leurs axones dans le cerveau, la moelle épinière ou le nerf optique, sert d’isolant électrique et permet une bonne conduction de l’influx nerveux. Mais lorsqu’elle se décompose sous l’assaut des LT, elle n’assure plus son rôle. L’information électrique ne passe plus : s’ensuivent des symptômes variant du simple engourdissement à la paralysie ou à la cécité.
Les traitements actuels visent à abaisser l’activité du système immunitaire afin qu’il épargne la gaine de myéline. En contrepartie, le patient voit augmenter ses risques de tomber malade. Cette thérapie n’est donc pas idéale.
© Selket, Wikipédia, cc by sa 3.0
La myéline est une gaine de lipides et de protéines qui se trouve dans les oligodendrocytes ou les cellules de Schwann, spécifiques au système nerveux. Elle recouvre les axones comme une gaine plastique protège les fils électriques, de façon à mieux conduire l’influx nerveux.
L’idée des scientifiques est de reprogrammer les LT défaillants. Ils semblent y parvenir d’après les résultats de tests cliniques de phases I et II. Le principe : des globules blancs d’un patient sont imprégnés des anticorps de la myéline et sont injectés dans la circulation. Les macrophages font leur travail, et cette fois, les lymphocytes apprennent correctement.
Cependant, une telle thérapie est très coûteuse (80.000 euros par personne). Alors des scientifiques de la Northwestern University (Chicago) ont remplacé ces globules blancs par des nanoparticules, bien moins chères à produire. Testées chez des souris atteintes d’une maladie équivalente à la sclérose en plaques, elles semblent aussi efficaces.
Des nanoparticules en PLG
Ces nanoparticules sont constituées de poly(lactide-co-glycolide) (ou PLG), un assemblage d’acides lactique et glycolique déjà validé par la Food and Drug Administration (FDA) et utilisé dans la plupart des sutures. Plongées une heure dans un bain chimique, elles s’imprègnent des antigènes caractéristiques de la myéline.
Comme expliqué dans Nature Biotechnology, ces nanoparticules de PLG sont ensuite injectées dans le sang des souris et transitent jusqu’à la rate, où elles sont avalées par les macrophages et considérées comme des cellules saines de l’organisme. Les antigènes sont présentés aux LT qui sont alors reconfigurés et épargneront les cellules de myéline.
Contre la sclérose en plaques… et d’autres maladies auto-immunes
Très vite, la maladie ne progresse plus. L’effet se produit sur le long terme, car plus de 100 jours après l’injection, les souris étaient toujours préservées. À l’échelle d’une vie d’Homme, cela équivaut à une dizaine d’années.
Seulement, on ignore encore s’il faudrait répéter régulièrement un tel traitement s’il prouvait son efficacité chez l’espèce humaine. Des études ultérieures le préciseront.
S’il bloque la maladie, le traitement ne répare pas le tissu abîmé. Ainsi, il conviendrait à des patients chez qui l’on détecte les tout premiers symptômes. Pour les patients plus atteints, il devra être utilisé en complément d’un autre traitement chargé de reconstituer les régions endommagées.
Le concept pourrait se généraliser et s’étendre à d’autres maladies auto-immunes. Il suffit de connaître l’antigène spécifique à présenter et, en théorie, on contrôlerait l’affection. On les connaît dans certaines pathologies, comme dans le diabète de type 1 ou pour certaines allergies, mais on ne sait pas quelle protéine utiliser dans le cas de la polyarthrite rhumatoïde par exemple. Il faudra encore creuser un peu…{jcomments off}
